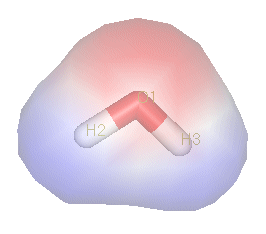
水分子
|
物理與化學性質:
水在常溫常壓下為無色無味的透明液體。在自然界,純水是罕見的,水通常多是含有酸、鹼、鹽等物質的溶液,習慣上仍然把這種水溶液稱為水。純水可以通過蒸餾作用取得,當然,這也是相對意義上純水,不可能絕對沒有雜質。水是一種可以在液態、氣態和固態之間轉化的物質。 在20℃時,水的熱導率為0.006 J/s·cm·K,冰的熱導率為0.023 J/s·cm·K,在雪的密度為0.1×103 kg/m3時,雪的熱導率為0.00029 J/s·cm·K。水的密度在3.98℃時最大,為1×103kg/m3,溫度高於3.98℃時,水的密度隨溫度升高而減小,在0~3.98℃時,水不服從熱脹冷縮的規律,密度隨溫度的升高而增加。水在0℃時,密度為0.99987×103 kg/m3,冰在0℃時,密度為0.9167×103 kg/m3。因此冰可以浮在水面上。 水的熱穩定性很強,當水蒸氣加熱到2000K以上時,也只有極少量的水離解為氫和氧,但水在通電的條件下(電解)會離解為氫和氧。具有很大的內聚力和表面張力,除汞以外,水的表面張力最大,並能產生較明顯的毛細現象和吸附現象。純水有極微弱的導電能力,但普通的水因含有少量電解質(如礦物質、溶解大氣中二氧化碳形成的碳酸)而有較強的導電能力。[來源請求] 水的三相點是273.16K(611.73Pa下),臨界點是647K(22.064 MPa下)。在臨界點之上水無法存在液相及固相,而在臨界點之下水蒸氣容易結成液相。 |
表面張力:
由於水具有所有非金屬液體中最大的表面張力值72.8 mN/m,使水滴保持相對穩定。當少量水滴滴在玻璃板上,即可觀察到水的表面張力:水滴繼續保持液滴狀態。另一個常見的例子是,向一杯注滿水的玻璃杯中緩緩投放硬幣,水不會立刻溢出,而是向上凸起。水的這一特性對生物來說非常重要。
例如,植物吸水時,水通過莖里的木質部向上運輸。強大的分子間作用力維持維管束中水的柱狀形態,粘接性使水柱聚集,粘性是水緊貼維管束壁,而張力則能防止葉面蒸散作用導致水柱斷裂。其他低張力的液體則會導致液柱裂開,形成真空,使蒸散作用失效。
由於水具有所有非金屬液體中最大的表面張力值72.8 mN/m,使水滴保持相對穩定。當少量水滴滴在玻璃板上,即可觀察到水的表面張力:水滴繼續保持液滴狀態。另一個常見的例子是,向一杯注滿水的玻璃杯中緩緩投放硬幣,水不會立刻溢出,而是向上凸起。水的這一特性對生物來說非常重要。
例如,植物吸水時,水通過莖里的木質部向上運輸。強大的分子間作用力維持維管束中水的柱狀形態,粘接性使水柱聚集,粘性是水緊貼維管束壁,而張力則能防止葉面蒸散作用導致水柱斷裂。其他低張力的液體則會導致液柱裂開,形成真空,使蒸散作用失效。
極性:
水的一項重要特性就是它的極性。水分子呈角狀,當中氫原子位於末端而氧原子則在頂點。由於氧的電負性比氫高,所以分子中有氧原子的一邊電荷會偏負。帶這樣一個電荷差的分子被稱為偶極子。
電荷差使得水分子互相吸引(偏正電的區域會被偏負電的區域吸引),同時亦使它們和其他極性分子互相吸引。這種吸引力被稱為氫鍵,它解釋了許多水的特性。某些分子,如二氧化碳,原子間負電性亦有差異,但不同之處在於二氧化碳分子形狀成對稱排列,因此對立電荷會被相互抵消。如果將電源靠近小水柱時亦可觀察到水的此一現象,這現象會使水向電源方向彎曲。
儘管氫鍵是一種相對較弱的引力(跟連接水分子內原子的共價鍵比較時),但是它造就了水的多個特性。其中一個特性就是水相對較高的熔點及沸點溫度,因為需要更多熱能才能夠克服分子間的氫鍵。相近的化合物硫化氫(H2S)的氫鍵較水的弱,即使它的質量是水的兩倍,在室溫下還是氣體。水分子間額外的鍵為液態水帶來了高比熱容。這種高比熱容使水成為一種較佳的熱量儲存媒介。
氫鍵也為水帶來了結冰時不尋常的表現。當被冷凍至冰點附近時,由於它們能透過重組來使能量最小化的關係,所以氫鍵的存在意味著分子可以形成帶六角形晶體結構的冰,這種冰的密度實際上較低:因此於固態時(冰)會浮水上。亦即是說,水結冰時會膨脹,而差不多其他全部物質凝固時都會沉下。
在足夠壓力下,固體密度比液體低會帶來一個有趣的效果。當壓力增加時熔點下降,而當熔點溫度比周圍環境低時冰會熔化。要使熔點大幅度下降需要增加相當大的壓力——溜冰者所施加的壓力只會把熔點下調約0.09 oC。
水的一項重要特性就是它的極性。水分子呈角狀,當中氫原子位於末端而氧原子則在頂點。由於氧的電負性比氫高,所以分子中有氧原子的一邊電荷會偏負。帶這樣一個電荷差的分子被稱為偶極子。
電荷差使得水分子互相吸引(偏正電的區域會被偏負電的區域吸引),同時亦使它們和其他極性分子互相吸引。這種吸引力被稱為氫鍵,它解釋了許多水的特性。某些分子,如二氧化碳,原子間負電性亦有差異,但不同之處在於二氧化碳分子形狀成對稱排列,因此對立電荷會被相互抵消。如果將電源靠近小水柱時亦可觀察到水的此一現象,這現象會使水向電源方向彎曲。
儘管氫鍵是一種相對較弱的引力(跟連接水分子內原子的共價鍵比較時),但是它造就了水的多個特性。其中一個特性就是水相對較高的熔點及沸點溫度,因為需要更多熱能才能夠克服分子間的氫鍵。相近的化合物硫化氫(H2S)的氫鍵較水的弱,即使它的質量是水的兩倍,在室溫下還是氣體。水分子間額外的鍵為液態水帶來了高比熱容。這種高比熱容使水成為一種較佳的熱量儲存媒介。
氫鍵也為水帶來了結冰時不尋常的表現。當被冷凍至冰點附近時,由於它們能透過重組來使能量最小化的關係,所以氫鍵的存在意味著分子可以形成帶六角形晶體結構的冰,這種冰的密度實際上較低:因此於固態時(冰)會浮水上。亦即是說,水結冰時會膨脹,而差不多其他全部物質凝固時都會沉下。
在足夠壓力下,固體密度比液體低會帶來一個有趣的效果。當壓力增加時熔點下降,而當熔點溫度比周圍環境低時冰會熔化。要使熔點大幅度下降需要增加相當大的壓力——溜冰者所施加的壓力只會把熔點下調約0.09 oC。
水分子對於生物學的重要性: 水在生物學中的重要性主要是因為生物在維持生理機能時需要仰賴水的物理及化學性質。
例如:植物在運送水分時,是利用水的氫鍵互相牽引所形成如水鏈狀結構,在植物專門運送水分的導管中形成氫鍵使水分子不會受到引力作用而掉落至導管管壁,再利用蒸散作用帶動水分向上運輸。在植物水分的運輸過程中充分的解釋了水的運輸牽涉於水的物理性質。
另外在生物體中,水是一種緩衝的溶液,利用解離出的氫氧基(OH-)以及質子(H+)可以將外來少量的強酸或強鹼中和,如此可確保細胞中的蛋白質結構的完整性,而對酵素而言,在酵素的結構上需要維持一定的結構才具有活性。而經由上述案例可說明在生物體內需要利用水的化學及物理性質才可維持生物體結構(細胞型狀)及機能(如酵素活性)上的穩定。
例如:植物在運送水分時,是利用水的氫鍵互相牽引所形成如水鏈狀結構,在植物專門運送水分的導管中形成氫鍵使水分子不會受到引力作用而掉落至導管管壁,再利用蒸散作用帶動水分向上運輸。在植物水分的運輸過程中充分的解釋了水的運輸牽涉於水的物理性質。
另外在生物體中,水是一種緩衝的溶液,利用解離出的氫氧基(OH-)以及質子(H+)可以將外來少量的強酸或強鹼中和,如此可確保細胞中的蛋白質結構的完整性,而對酵素而言,在酵素的結構上需要維持一定的結構才具有活性。而經由上述案例可說明在生物體內需要利用水的化學及物理性質才可維持生物體結構(細胞型狀)及機能(如酵素活性)上的穩定。